
músculo relaxado
O músculo pode ser comparado a uma máquina que transforma energia química em
trabalho, produzindo calor. Quando em atividade, pode alterar sua tensăo e seu
comprimento. As propriedades fisiológicas dos músculos săo diferentes nos diferentes
estados: relaxamento, início da contraçăo, contraçăo propriamente dita e retorno ao
relaxamento.
A força exercida pelo músculo na contraçăo é medida pela unidade de tensăo (P),
que permite a correçăo para o tamanho do músculo (medida pela área de maior secçăo
transversal do músculo em questăo). O tamanho do músculo é expresso como uma fraçăo
do comprimento do músculo em que ele é capaz de exercer maior tensăo isométrica (lo)
.
Um músculo relaxado pode ser estendido até certo comprimento, quando entăo oferece
resistęncia ao aumento do comprimento. Esta resistęncia caracteriza a existencia de um
componente elástico no músculo em repouso. No entanto, quando um músculo é estimulado
tetanicamente năo se permitindo a mudança de comprimento (contraçăo isométrica),
observa-se a situaçăo de tensăo máxima. A tensăo varia muito conforme o estado do
músculo (relaxado, pouco contraído, muito contraído, contraçăo máxima). No caso de
um músculo contraído ao máximo, a velocidade de contraçăo é zero [peso infinito].
Quando diminuimos o peso aplicado ao músculo, existirá um peso no qual a velocidade de
contraçăo pode ser observada (mas ainda é mínima e constante). Se o peso for
diminuído gradativamente (diminuindo assim a tensăo exercida pelo músculo), a
velocidade de contraçăo irá aumentando proporcionalmente (peso próximo de zero implica
em velocidade de contraçăo máxima).
Contraçăo isotônica: aquela em que a velocidade é diferente de zero e a tensăo é
constante. A produçăo de calor por um músculo em contraçăo isotônica é proporcional
ŕ mudança de comprimento do músculo e năo depende da velocidade de contraçăo ou do
peso que foi levantado. Nas contraçőes isoméricas, onde năo há alteraçăo do
comprimento do músculo, existe a liberaçăo de calor de manutençăo. Esta quantidade de
calor é proporcional ao tamanho do músculo e corresponde ŕ energia necessária para
manter a tensăo.
Quando parte de um músculo está envolvido na manutençăo da tensăo, esta parte năo
estaria necessariamente impedida de participar na geraçăo de calor.
Estrutura Molecular:
Num músculo estriado esquelético típico, encontramos um eixo principal que liga os
dois tendőes, presos ao osso a nível da articulaçăo. As células musculares se
orientam ao longo deste eixo, săo células multinucleadas envoltas individualmente por
tecido conjuntivo pelo qual chegam vasos capilares e nervos. O músculo contendo estas
células é envolvido por um tecido conjuntivo mais grosso.
Dentro das células musculares encontram-se feixes de estruturas quase tăo longas
quanto a própria célula (miofibrilas). Na célula muscular podem ser observados dois
compartimentos individualizados: um contem miofribrilas, mitocôndrias e lisossomas. O
segundo, delimitado pelo retículo sarcoplasmático, năo contem organelas.
A miofibrila apresenta uma alternância de bandas claras e escuras ao microscópio
óptico. As bandas claras năo apresentam birrefringęncia e săo portanto isotrópicas
(bandas I) e as bandas escuras, birrefringentes săo anisotrópicas (bandas A). Esta
sequęncia de bandas se repete pela miofibrila ao longo do seu comprimento - cada unidade
é chamada sarcômero (vai da metade da banda I até a metade da banda I seguinte). Este
ponto de metade da banda I é marcado pela presença de um disco mais escuro, chamado
linha ou disco Z. Da mesma forma, na metada das bandas A existe um área de coloraçăo
mais clara chamada banda H. A banda A é formada por miosina e a banda I por actina.
Esquematicamente:

músculo relaxado
O ATP é responsável pelo fornecimento de energia para a contraçăo muscular.
Miofibrilas isoladas podem ser contraídas e observadas no microscópio comum na presença
de ATP. Durante a contraçăo a banda I diminui de comprimento e a banda A permanece com
aproximadamente o mesmo comprimento. As bandas Z se aproximam.
Na ausęncia de ATP, a actina e a miosina permanecem ligadas. Na presença de ATP
ocorre hidrólise da junçăo [ponte] miosina/actina, a energia liberada por esta
hidrólise faz com que um filamento se desloque sobre o outro.
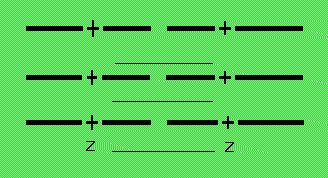
músculo contraído
Este modelo, chamado "filamentos deslizantes", propőe que o músculo se
contraia através do deslizamento de dois filamentos um sobre o outro, sem que nenhum dos
dois altere sua estrutura, composiçăo química ou comprimento.
Na contraçăo muscular isotônica observa-se uma diminuiçăo no comprimento do
sarcômero e os filamentos tendem a se encontrar no centro da banda H. Neste ponto, existe
tensăo máxima e năo há como deslizar mais os filamentos, atingindo uma situaçăo
isométrica. No caso da contraçăo isométrica [tetânica], onde năo observa
diminuiçăo do comprimento do músculo, a energia liberada pelo ATP năo pode ser
transformada em trabalho devido ŕ incapacidade de deslizar mais os filamentos sobre os
outros e há produçăo de calor mas năo de trabalho. A tensăo seria entăo determinada
pelas pontes.
A quantidade de ATP hidrolisada é proporcional ŕ reciclagem das pontes . Qaundo a
contraçăo é realizada com alta velocidade e baixa tensăo, a reciclagem de pontes é
alta e mais quantidade de ATP é necessária. Ŕ medida que a velocidade diminui, a
reciclagem de pontes é mais lenta e e menos ATP é consumido, mesmo que a tensăo seja
aumentada.
Bases moleculares da pontes:
Miosina:
A miosina é uma molécula longa com uma cauda e duas cabeças. As cabeças podem se
mover em relaçăo a si mesmas e em relaçăo ŕ cauda. Miosina pode ser separada por
enzimas proteolíticas em dois pontos diferentes. Se tratada com tripsina, a miosina é
dividida em meromiosina pesada [fragmento que retem a atividade ATPásica] e meromiosina
leve [que năo possui atividade enzimática]. Meromiosina pesada é solúvel em baixas
concentraçőes de sal enquanto o fragmento meromiosina leve só é solúvel em
concentraçőes salinas bastante altas. A meromiosina pesada pode ainda ser clivada em
dois fragmentos pela papaína, um chamado subfragmento S-1 [que retem atividade ATPásica]
e o subfragmento S-2 sem atividade enzimática.
Para estudo dos polipeptídeos que compőem a estrutura quaternária da miosina, basta
romper as pontes dissulfeto e proceder a eletroforese para separaçăo por peso molecular.
Existem duas cadeias pesadas na cauda e dois ou tręs pares de cadeias leves nas cabeças.
As cadeias leves estariam relacionadas ŕ atividade ATPásica. O peso molecular e o
número destas cadeias leves variam de acordo com o músculo estudado e o tipo de fibras
[rápidas ou lentas].
Magnésio é o único cátion com efeito acelerador da atividade ATPásica da miosina.
O substrato realmente hidrolisado pela miosina parece ser Mg-ATP. A actina estimula de
forma significativa a hidrólise de ATP, e in vivo, a interaçăo destas duas proteínas
deve ser o fenômeno responsável pela hidrólise do ATP durante uma contraçăo.
Actina:
A actina é uma proteína globular com uma única cadeia polipeptídica e peso
molecular de 45KD. No estado monomérico (actina-G), possui uma molécula de ATP e uma de
cálcio incorporadas em sua estrutura. Em soluçăo de alta força iônica, a actina se
polimerizará, ficando filamentosa com uma dupla fileira de monômeros enrolados sobre si
mesmos. Na passagem da forma monomérica para a forma filamentosa, o ATP é hidrolizado.
Actina/Miosina: se colocadas juntas numa soluçăo, com o passar do tempo a soluçăo
se torna mais viscosa [formaçăo de complexos actina/miosina] e há aumento de fosfato
livre ŕs custas da diminuiçăo de ATP. O ADP formado é estável. A queda de ATP mantem
as moléculas de actina e miosina juntas e colocaçăo de novo ATP na soluçăo diminui
sua viscosidade.
Durante a contraçăo e distensăo de uma célula muscular năo ocorre um deslizamento
livre sobre os dois tipos de filamentos. No relaxamento, uma lenta hidrólise de ATP
ocorre e mantem uma certa tensăo entre os filamentos. Com a constante regeneraçăo de
ATP, năo se observa um estado de inextensibilidade das fibras musculares, a năo ser nos
casos de rigor mortis, onde năo existe novo influxo de ATP para o complexo. A
concentraçăo de ATP se mantem constante devido ŕ regeneraçăo a partir de ADP e
fosfocreatina, reaçăo catalisada pela creatinoquinase.
Uma fibra em contraçăo isométrica em um dado comprimento, responde com mudança de
seu comprimento em alguns milisegundos, e se estabiliza na nova situaçăo. A alteraçăo
por que passa a tensăo nesse tempo é chamada de um “transiente”. No transiente
observa-se que a tensăo varia de forma linear com a mudança de comprimento, até atingir
um plateau.
Regulaçăo da contraçăo muscular:
Em 1947 foi demonstrado que a injeçăo de pequenas quantidades de Ca++ numa fibra
muscular desencadeava contraçăo năo só no local mas propagada por grande parte da
fibra. Devido ao curto tempo que se observa entre a despolarizaçăo da membrana
plasmática e a contraçăo muscular, concluiu-se que năo se tratava de um simples
processo de despolarizaçăo e difusăo de íons pela membrana.
Atualmente sabe-se que com micropipetas suficientemente finas, pode-se estudar a
contraçăo de determinados segmentos da fibra e estimular áreas tăo restritas quanto
bandas A, I e Z, dependendo da especialidade do músculo e do animal em questăo. A
membrana plasmática das fibras musculares é composta por um tubo cercado por duas
vesículas de retículo endoplasmático liso e que circunda toda as miofibrilas. Este
túbulo é o túbulo em T pois se coloca perpendicularmente ŕ membrana plasmática.
O estímulo elétrico é levado ao interior da fibra muscular através dos túbulos e
as bolsas de Ca++ encontradas no interior do retículo estăo tăo próximas da unidade
contrátil que o espaço de tempo necessário entre o estímulo e a contraçăo pode ser
explicado desta forma [e năo por difusăo de íons, conforme se pensava originalmente].
Terminada a onda de despolarizaçăo, o calcio é ativamente rebombeado para dentro do
retículoe o músculo relaxa. A regulaçăo da contraçăo muscular depende portanto do
nível de calcio nas miofibrilas e năo da quantidade de ATP presente. Como a bomba de
calcio é ATP-dependente, conclui-se que mesmo o processo de relaxamento exige gasto de
energia.
Subunidades da Actina:
A actina pura na verdade năo tem grande sensibilidade ao cálcio e foram as outras
moléculas isoladas de preparaçőes purificadas de músculos que mostraram uma capacidade
maior de regulaçăo pelo cálcio. Estas duas proteínas responsáveis pela sensibilidade
do complexo ao cálcio costumavam contaminar as preparaçőes iniciais de actina, mas hoje
sabe-se que săo proteínas independentes. A 1a destas proteínas é a tropomiosina
(filamentosa) e a segunda é a troponina (globular). A troponina pode ser dividida em 3
subunidades. A 1a, que apresenta ligaçőes relativamente estáveis com a tropomiosina, é
chamada TN-T. A 2a subunidade tem grande capacidade de inibir a ATPase da actomiosina in
vitro e é chamada TN-I. A 3a subunidade tem como principal característica sua afinidade
com o cálcio e é denominada TN-C. Assim, cada molécula de troponina contem 3
subunidades, uma que mantem a ligaçăo com a tropomiosina, outra que inibe as reaçőes
da ATPase e outra responsável pela ligaçăo com o calcio.
Acredita-se que nos sulcos formados entre duas fileiras de actina enroladas sobre si
mesmas, se coloquem moléculas de tropomiosina. Cada molécula de tropomiosina estaria em
contato com 7 moléculas de actina. Ligada a cada molécula de tropomiosina estaria uma
molécula de troponina. Na ausęncia de calcio, as subunidades TN-I e TN-T impediriam
(devido ŕ sua localizaçăo) a ligaçăo da actina e da miosina, impedindo assim a
contraçăo muscular. Quando o calcio fosse liberado , ele se ligaria ŕ subunidade TN-C
deslocando a molécula de tropomiosina. Assim estariam liberados os sítios de ligaçăo
actina/miosina. Quando o calcio fosse rebombeado para o retículo sarcoplasmático, a TN-C
perderia sua ligaçăo e a molécula de tropomiosina se deslocaria novamente agora
impedindo que os os sítios de ligaçăo actina/miosina ficassem livres.
Este sistema de contraçăo muscular estaria constantemente "armado" e por
isso a descarga elétrica desencadearia uma resposta tăo rápida.
Em resumo:
| transmissăo sináptica gera despolarizaçăo levada ao interior da fibra pelos túbulos
em T. | |
| liberaçăo de calcio armazenado no interior de vesículas | |
| calcio + TN-C = alteraçăo conformacional da troponina | |
| deslocamento da tropomiosina = libera os sítios de ligaçăo actina/miosina | |
| bomba de calcio retorna o calcio para o retículo sarcoplasmático (uso de ATP) | |
| TN-C perde o calcio = troponina e tropomiosina retornam ao estado anterior |